
Fig 1. Salvinorina-A en diferentes niveles de pureza usando nafta y alcohol isopropílico.
La salvinorina-A es un diterpenoide trans-neoclerodano. Taxonómicamente, pertenece al reino de los compuestos orgánicos, a la superclase de los lípidos y sustancias lipoides, a la clase de lípidos prenoles y a la subclase de lactonas terpénicas. Su fórmula química es C23H28O8. Es un diterpenoide por la cantidad de átomos de carbono que posee derivados de la condensación de cuatro unidades de isoprenilo.[1] Es un trans-neoclerodano debido a su estereoquímica, es decir, a la posición y distribución de sus átomos en el espacio que componen la molécula diterpenoide,[2] específicamente por poseer cuatro estereocentros contiguos. La salvinorina-A tiene un peso molecular de 432.464 g/mol. Un punto de fusión de 240°C y un punto de ebullición de 760.2°C. Es una sustancia lipofílica con un coeficiente de reparto de 2.49. Tiene 7 centros quirales, de los cuales 3 carbonos son epimerizables.[3]
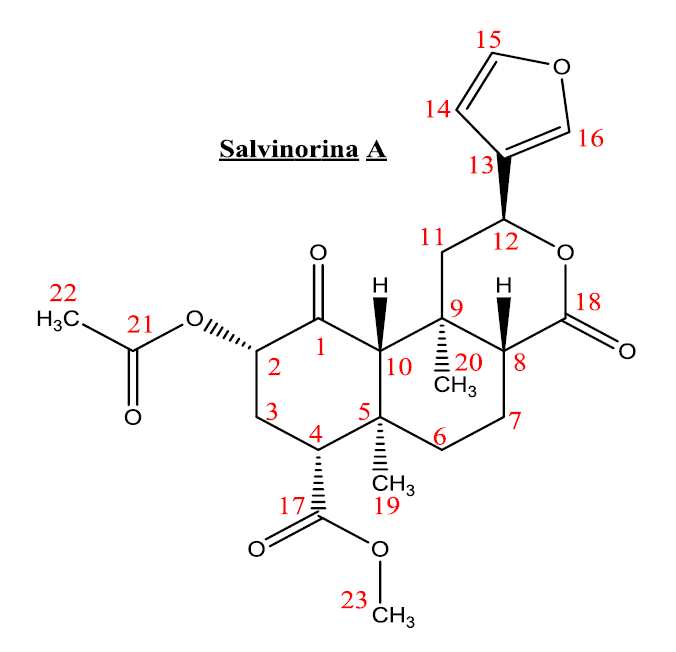
Fig 2. Estructura molecular de la salvinorina-A
Desde el punto de vista estructural, la salvinorina-A es una molécula que está compuesta principalmente por un núcleo terpénico que contiene 3 anillos de seis miembros. Con el fin de puntualizar aquellas características estructurales se van a mencionar los grupos funcionales de mayor relevancia: En la posición 2 (C-2) hay un grupo acetoxi, en la posición 4 (C-4) un metilester y en la posición 12 (C-12) se encuentra un anillo furanico. En la posición 17 (C-17) se encuentra un éster y en la posición 1 (C-1) una cetona.[4] Su nombre IUPAC es: metil (2S,4aR,6aR,7R,9S,10aS,10bR)-9-acetiloxi-2-(furan-3-ilo)-6a,10b-dimetil-4,10,dioxo-2,4a,5,6,7,8,9,10a-octahidro-1H-benzo[f]isocromeno-7-carboxilato. Tiene un área de supericie polar topológica de 109.11 Ų , una refractividad de 106 m3·mol-1 y una polarizabilidad de 44.17 Å3. Tiene una muy baja solubilidad en agua de 12.1 mg/L a 25°C.
El químico mexicano Alfredo Ortega fue el primero en aislar salvinorina-A de Salvia divinorum en 1982. Utilizó cloroformo para extraer salvinorina-A de hojas secas, arcilla activada Tonsil para el proceso de cromatografía y metanol para el proceso de cristalización.[5] Daniel Siebert comprobó que la salvinorina-A se encuentra concentrada principalmente en tricomas glandulares peltados ubicados en la cara inferior (envés) de las hojas de Salvia divinorum, con mayor densidad en hojas recién formadas y con una distribución más amplia en hojas maduras.[6]

Fig 3. Dr. Alfredo Ortega, primer químico en extraer e identificar la salvinorina-A
El químico australiano Thomas Anthony Munro es uno de los expertos más informados en el tema de la salvinorina-A y moléculas relacionadas. Su publicación “The Chemistry of Salvia divinorum” (2006) es uno de los documentos más completos acerca de la química de la salvinorina-A y los varios diterpenoides que contiene la Salvia divinorum. Además, Munro y su equipo son los responsables de la creación de la molécula semi-sintética, 2-Etoximetil-eter-Salvinorina-B[7], mejor conocida como Symmetry, la cual es por lo menos 5 veces más potente que la salvinorina-A en términos farmacológicos.[8]
La salvinorina-A es soluble en disolventes orgánicos como la acetona, el acetonitrilo, el cloroformo y el metanol.[9] Cualquiera de estos disolventes son útiles para poder realizar una extracción exitosa de salvinorina-A a partir de hojas de Salvia divinorum, siendo la acetona la opción preferida por amateurs debido a la fácil accesibilidad y manejo de este compuesto. Es importante mencionar que la extracción cruda de salvinorina-A se diferencía de la extracción pura en el sentido de que la cruda es más sencilla pero mantiene las impurezas (principalmente clorofila) y la pura las elimina gracias a refinamiento con nafta o 99% alcohol isopropílico, pero reduciendo proporcionalmente la cantidad de salvinorina-A obtenida en el peso final.
Fuentes:
- “Diterpenoids from de the Medicinal Plants of Africa”, Sandjo & Kuete, 2013.
- “Clerodane diterpenes: sources, structures, and biological activities”, Li, et al. 2016
- “Salvinorin A: A Mini Review of Physical and Chemical Properties Affecting Its Translation from Research to Clinical Applications in Humans”, Orton & Liu, 2014
- “Purificación, caracterización e identificación de Salvinorina A en Salvia divinorum”, Huérfano, 2015.
- “Salvinorin, A New trans-Neoclerodane Diterpene from Salvia divinorum (Labiatae)”, Ortega, 1982.
- “Localization of Salvinorin A and Related Compounds in Glandular Trichomes of the Psychoactive Sage, Salvia divinorum”, Siebert, 2004.
- “Standard Protecting Groups Create Potent and Selective Kappa Opioids: Salvinorin B Alkoxymethyl Ethers” Munro, et al. 2007
- “First Look at a New Psychoactive Drug: Symmetry (salvinorin B ethoxymethyl ether)”. Mercury & Feelood, The Entheogen Review. 2008.
- “Farmacología humana de la salvinorina A: estudio de mecanismo de acción central mediante bloqueo farmacológico de los efectos” – Maqueda, 2018



